Клинический случай диагностики и комплексного лечения наружного генитального эндометриоза у пациентки с бесплодием
- Резюме
- Для цитирования
- Авторы
- Abstract
- Полный текст
- Литература
- Smolarz B., Szyłło K., Romanowicz H. Endometriosis: epidemiology, classification, pathogenesis, treatment and genetics (review of literature). Int. J. Mol. Sci. 2021;22(19):10554. DOI: 10.3390/ijms221910554
- Filip L., Duică F., Prădatu A., Crețoiu D. et al. Endometriosis associated infertility: a critical review and analysis on etiopathogenesis and therapeutic approaches. Medicina. 2020;56(9):460. DOI: 10.3390/medicina56090460
- Moss K.M., Doust J., Homer H., Rowlands I.J. et al. Delayed diagnosis of endometriosis disadvantages women in ART: a retrospective population linked data study. Hum. Reprod. 2021;36(12):3074–82. DOI: 10.1093/humrep/deab216
- Dunselman G.A.J., Vermeulen N., Becker C., Calhaz-Jorge C. et al. ESHRE guideline: management of women with endometriosis. Hum. Reprod. 2014;29(3):400–12. DOI: 10.1093/humrep/det457
- Byrne D., Curnow T., Smith P., Cutner A. et al. Laparoscopic excision of deep rectovaginal endometriosis in BSGE endometriosis centres: a multicentre prospective cohort study. BMJ Open. 2018;8(4):e018924. DOI: 10.1136/bmjopen-2017-018924
- Bafort C., Beebeejaun Y., Tomassetti C., Bosteels J. et al. Laparoscopic surgery for endometriosis. Cochrane Database Syst. Rev. 2020;10(10):CD011031. DOI: 10.1002/14651858.CD011031.pub3
- Becker C.M., Bokor A., Heikinheimo O., Horne A. et al. ESHRE guideline: endometriosis. Hum. Reprod. Open. 2022;2022(2):hoac009. DOI: 10.1093/hropen/hoac009
- Horne A.W., Missmer S.A. Pathophysiology, diagnosis, and management of endometriosis. BMJ. 2022;379:e070750. DOI: 10.1136/bmj-2022-070750
- Taylor H.S., Kotlyar A.M., Flores V.A. Endometriosis is a chronic systemic disease: clinical challenges and novel innovations. Lancet. 2021;397(10276):839–52. DOI: 10.1016/S0140-6736(21)00389-5
- Revised American Society for Reproductive Medicine classification of endometriosis: 1996. Fertil. Steril. 1997;67(5):817–21. DOI: 10.1016/s0015-0282(97)81391-x
- Adamson G.D., Pasta D.J. Endometriosis fertility index: the new, validated endometriosis staging system. Fertil. Steril. 2010;94(5):1609–15. DOI: 10.1016/j.fertnstert.2009.09.035
- Nisenblat V., Bossuyt P.M., Farquhar C., Johnson N. et al. Imaging modalities for the non-invasive diagnosis of endometriosis. Cochrane Database Syst. Rev. 2016;2016(2):CD009591. DOI: 10.1002/14651858.CD009591.pub2
- Wykes C.B., Clark T.J., Khan K.S. Accuracy of laparoscopy in the diagnosis of endometriosis: a systematic quantitative review. BJOG. 2004;111(11):1204–12. DOI: 10.1111/j.1471-0528.2004.00433.x
- Сергиеня О.В., Юхно Е.А., Павловская Е.А., Фокин В.А. и др. Возможности магнитно-резонансной томографии в визуализации структурных изменений органов малого таза у женщин репродуктивного возраста при бесплодии. Российский электронный журнал лучевой диагностики. 2018;8(1):119–28. Sergienya O.V., Yukhno E.A., Pavlovskaya E.A., Fokin V.A. et al. Magnetic resonance imaging in visualization of structural changes in the pelvic organs in women of reproductive age with infertility. Russian Electronic Journal of Radiology. 2018;8(1):119–28. (in Russian). DOI:10.21569/2222-7415-2018-8-1-119-128
- Foti P.V., Farina R., Palmucci S., Vizzini I.A.A. et al. Endometriosis: clinical features, MR imaging findings and pathologic correlation. Insights Imaging. 2018;9(2):149–72. DOI: 10.1007/s13244-017-0591-0
- Kido A., Himoto Y., Moribata Y., Kurataet Y. et al. MRI in the diagnosis of endometriosis and related diseases. Korean J. Radiol. 2022;23(4):426–45. DOI: 10.3348/kjr.2021.0405
- Bosch E., Broer S., Griesinger G., Grynberg M. et al. ESHRE guideline: ovarian stimulation for IVF/ICSI. Hum. Reprod. Open. 2020;2020(2):hoaa009. DOI: 10.1093/hropen/hoaa009
- Zhao F., Lan Y., Chen T., Xin Z. et al. Live birth rate comparison of three controlled ovarian stimulation protocols for in vitro fertilization-embryo transfer in patients with diminished ovarian reserve after endometrioma cystectomy: a retrospective study. J. Ovarian Res. 2020;13(1):23. DOI: 10.1186/s13048-020-00622-x
- Ata B., Telek S.B. Assisted reproductive technology for women with endometriosis, a clinically oriented review. Curr. Opin. Obstet. Gynecol. 2021;33(3):225–31. DOI: 10.1097/GCO.0000000000000710
- Doğan Durdağ G., Çağlar Aytaç P., Alkaş Yağınç D., Yetkinel S. et al. Comparison of fixed and flexible progestin-primed ovarian stimulation protocols to prevent premature luteinization in patients with diminished ovarian reserve. Arch. Gynecol. Obstet. 2023;308(2):579–86. DOI: 10.1007/s00404-023-07071-z
- Du M., Zhang J., Li Z., Liu X. et al. Comparison of the cumulative live birth rates of progestin-primed ovarian stimulation and flexible GnRH antagonist protocols in patients with low prognosis. Front. Endocrinol. 2021;12:705264. DOI: 10.3389/fendo.2021.705264
- Iwami N., Kawamata M., Ozawa N., Yamamoto T. et al. New treatment strategy for endometriosis using progestin-primed ovarian stimulation with dienogest: a prospective cohort study, comparison of dienogest versus dydrogesterone. Reprod. Biol. 2021;21(1):100470. DOI: 10.1016/j.repbio.2020.100470
- Yang A.-M., Feng T.-F., Han Y., Zhao Z.-M. et al. Progestin-primed ovarian stimulation protocol for patients with endometrioma. Front. Endocrinol. 2022;13:798434. DOI: 10.3389/fendo.2022.798434
- Chung M.S., Han S.J. Endometriosis-associated angiogenesis and anti-angiogenic therapy for endometriosis. Front. Glob. Women’s Health. 2022;3:856316. DOI: 10.3389/fgwh.2022.856316
- Kim H.J., Kim S.H., Oh Y.S., Lee S.R. et al. Dienogest may reduce estradiol- and inflammatory cytokine-induced cell viability and proliferation and inhibit the pathogenesis of endometriosis: a cell culture- and mouse model-based study. Biomedicines. 2022;10(11):2992. DOI: 10.3390/biomedicines10112992
- Chapron C., Marcellin L., Borghese B., Santulli P. Rethinking mechanisms, diagnosis and management of endometriosis. Nat. Rev. Endocrinol. 2019;15(11):666–82. DOI: 10.1038/s41574-019-0245-z
- Grady R., Alavi N., Vale R., Khandwala M. et al. Elective single embryo transfer and perinatal outcomes: a systematic review and meta-analysis. Fertil. Steril. 2012;97(2):324–31. DOI: 10.1016/j.fertnstert.2011.11.033
Цель статьи: представить клинический случай диагностики и комплексного лечения эндометриоза у пациентки с бесплодием.
Основные положения: Проблема бесплодия, связанного с эндометриозом, крайне актуальна. Важное направление — поиск наиболее эффективного неинвазивного метода диагностики эндометриоза, т. к. проведение лапароскопии только с диагностической целью приводит к увеличению числа ненужных хирургических вмешательств. Формирование единой тактики ведения пациенток с эндометриозом — еще одна задача, которая стоит перед специалистами репродуктивной медицины. Лечение бесплодия и болевого синдрома при эндометриозе далеко не всегда можно провести одновременно.
Заключение. Магнитно-резонансная томография в руках опытного специалиста может стать ключевым методом неинвазивной диагностики эндометриоза. Комплексный подход к лечению бесплодия и эндометриоза позволяет в короткие сроки определиться с тактикой, купировать болевой синдром, а также помочь женщине достичь желанной беременности.
Ключевые слова: вспомогательные репродуктивные технологии, клинический случай, лечение бесплодия, репродуктивная медицина, эндометриоз
Скачать PDFЕфимова А.А., Горелова И.В., Маколкин А.А., Сергиеня О.В., Зазерская И.Е. Клинический случай диагностики и комплексного лечения наружного генитального эндометриоза у пациентки с бесплодием. Женское здоровье и репродукция. 2023. № 3 (58). URL: https://journalgynecology.ru/statyi/klinicheskij-sluchaj-diagnostiki-i-kompleksnogo-lechenija-naruzhnogo-genitalnogo-jendometrioza-u-pacientki-s-besplodiem/ (дата обращения: дд.мм.гггг)
Ефимова Алёна Александровна (автор для переписки) — ассистент кафедры акушерства и гинекологии с клиникой ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2. eLIBRARY.RU SPIN: 2423-0370. https://orcid.org/0000-0003-3323-1561. E-mail: alyona-sokolova@mail.ru
Горелова Инга Вадимовна — к. м. н., доцент кафедры акушерства и гинекологии с клиникой ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России; заведующая отделением вспомогательных репродуктивных технологий ООО «Дельта фертилити клиник». 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2. eLIBRARY.RU SPIN: 1207-5705. E-mail: ingavgorelova@gmail.com
Маколкин Александр Александрович — к. м. н., врач акушер-гинеколог ООО «Дельта фертилити клиник». 199034, Россия, г. Санкт-Петербург, 13-я линия Васильевского острова, д. 10. https://orcid.org/0000-0001-8858-7333. E-mail: amakolkin@df.clinic
Сергиеня Ольга Валерьевна — к. м. н., врач-рентгенолог отделения магнитно-резонансной томографии ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2. eLIBRARY.RU SPIN: 1637-1025. https://orcid.org/0000-0002-6495-700X. E-mail: mrtsergienya@mail.ru
Зазерская Ирина Евгеньевна — д. м. н., профессор, заведующая кафедрой акушерства и гинекологии с клиникой ИМО, руководитель профильных отделений университетской клиники ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2. eLIBRARY.RU SPIN: 5683-6741. https://orcid.org/0000-0003-4431-3917. Е-mail: zazera@mail.ru
A clinical case of diagnosis and complex treatment of endometriosis in a patient with infertility
A.A. Efimova1, I.V. Gorelova1, 2, A.A. Makolkin2, O.V. Sergienya1, I.E. Zazerskaya1
1 Almazov National Medical Research Centre; 2 Akkuratov Str., Saint Petersburg, Russian Federation 197341
2 Delta Fertility Clinic; 10 13th Line of Vasil`evskiy island, Saint Petersburg, Russian Federation 199034
Abstract
The purpose of the article: to present a clinical case of diagnosis and complex treatment of endometriosis in a patient with infertility.
Key points: the problem of infertility associated with endometriosis is extremely relevant. An important direction is the search for the most effective non-invasive method for diagnosing endometriosis, because performing laparoscopy only for diagnostic purposes leads to an increase in the number of unnecessary surgical interventions. The formation of a unified management strategy for patients with endometriosis is another task that reproductive medicine specialists face. Treatment of infertility and pain in endometriosis cannot always be carried out simultaneously.
Conclusion. Magnetic resonance imaging (MRI) can be a key method of non-invasive diagnosis of endometriosis. An integrated approach to the treatment of infertility and endometriosis allows to determine the tactics, stop the pain syndrome, and achieve the desired pregnancy.
Key words: clinical case, endometriosis, infertility treatment, reproductive medicine, ART.
А.А. Ефимова*1, И.В. Горелова1, 2, А.А. Маколкин2, О.В. Сергиеня1, И.Е. Зазерская1
1 ФГБУ «Национальный медицинский исследовательский центр имени В.А. Алмазова» Министерства здравоохранения Российской Федерации; Россия, г. Санкт-Петербург
2 ООО «Дельта фертилити клиник»; Россия, г. Санкт-Петербург
Эндометриоз — это хроническое воспалительное заболевание, при котором отмечаются наличие и рост дисфункциональных эндометриоподобных желез и стромы, часто с реактивным фиброзом и мышечной метаплазией, вне матки [1]. Наружный генитальный эндометриоз выявляется в среднем у 50% женщин, страдающих бесплодием, и является одной из основных причин отсутствия беременности [2].
При этом диагностика заболевания по-прежнему представляет сложность для врачей: среднее время от появления симптомов до выявления эндометриоза — 8–10 лет [1, 3]. Если у женщины с эндометриозом нет яркой клинической картины и/или характерных ультразвуковых признаков (например, эндометриоидных кист яичника), то в большинстве случаев диагноз эндометриоза не устанавливается, и пациенток ведут по алгоритму лечения бесплодия неясного генеза [3].
Для диагностики наружного генитального эндометриоза «золотым стандартом» долгое время была лапароскопия [4]. Однако проведение диагностической операции у всех пациенток с бесплодием неясного генеза ведет к увеличению количества неоправданных хирургических вмешательств и риска послеоперационных осложнений [5, 6]. С развитием лучевых методов диагностики инвазивные процедуры, проводимые исключительно с диагностической целью, должны осуществляться все реже. Европейское общество репродукции человека и эмбриологии (European Society of Human Reproduction and Embryology, ESHRE) рекомендует чаще использовать методы визуализации для диагностики эндометриоза и больше не считает лапароскопическое подтверждение обязательным для постановки диагноза [7].
Тазовая боль и бесплодие у женщин репродуктивного возраста — самые частые клинические проявления данного заболевания, которые оказывают выраженное влияние на качество жизни и требуют медицинского вмешательства [1, 8, 9]. При этом лечение данных симптомов у пациенток с эндометриозом далеко не всегда можно провести одновременно. Мы представляем клинический случай диагностики бесплодия, связанного с эндометриозом, и выбора тактики лечения, которая позволила максимально быстро и эффективно купировать болевой синдром у пациентки и преодолеть бесплодие.
Клиническое наблюдение
Пациентка 31 года обратилась в клинику вспомогательных репродуктивных технологий (ВРТ) «Дельта фертилити клиник» с жалобами на отсутствие беременности при регулярной половой жизни без контрацепции в течение 4 лет.
Ранее она прошла обследование, не выявившее причины отсутствия беременности (маточные трубы проходимы, по данным гистеросальпингографии, менструальный цикл овуляторный, у партнера — нормозооспермия), и ей установили диагноз бесплодия неясного генеза (N97.9). У пациентки выполнены три попытки искусственной инсеминации спермой партнера в естественном цикле, которые не привели к наступлению беременности.
Из анамнеза известно: менструации с 15 лет по 4–5 дней, через 28 дней, регулярные, обильные, болезненные — до 7–8 баллов по визуальной аналоговой шкале боли (ВАШ), нарушение стула во время менструации. Женщина жаловалась на болезненность при половом акте (глубокую диспареунию). Беременностей не было. Гормональную контрацепцию не применяла.
При объективном осмотре: рост 172 см, масса — 56 кг, индекс массы тела — 18 кг/м2 (дефицит массы тела), конституция астеническая. При гинекологическом осмотре на кресле, в зеркалах и при бимануальном обследовании патология органов малого таза не обнаружена, однако пациентка отмечала болезненность при тракциях за шейку матки.
При ультразвуковом исследовании (УЗИ) органов малого таза, проведенном на 17-й день менструального цикла, признаки патологии органов малого таза не выявлены.
Данные лабораторного обследования: уровень фолликулостимулирующего гормона — 5,51 МЕ/л, антимюллерова гормона (АМГ) — 3,2 нг/мл, содержание пролактина, тиреотропного гормона — в пределах нормальных значений. Результат спермограммы партнера: объем — 3,5 мл, концентрация — 24 млн/мл, концентрация прогрессивно-подвижных сперматозоидов (А + В) — 34%, нормальных форм — 3%, MAR-тест отрицательный.
С учетом жалоб женщины на болезненные менструации, а также данных бимануального осмотра было заподозрено наличие эндометриоза и рекомендовано проведение комплексной магнитно-резонансной томографии (МРТ) органов малого таза.
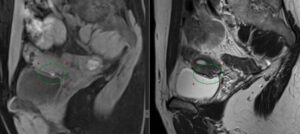
По результатам МРТ, найдены признаки функциональных геморрагических кист левого яичника; эндометриоидных фиброзных включений в ретроцервикальном пространстве (преимущественно в срединно-правых отделах) с вовлечением правой маточно-крестцовой связки, в маточно-пузырном углублении (без признаков инвазивного роста) и в области левой маточной трубы (рис. 1 А, В; 2 А, В; 3 А, В).
Ввиду жалоб на бесплодие и хроническую тазовую боль у пациентки выполнена лапароскопическая операция.
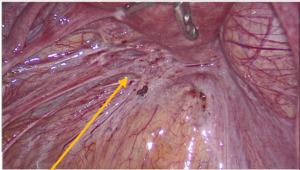
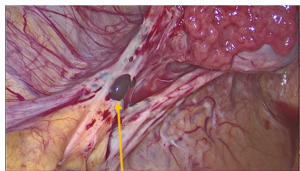
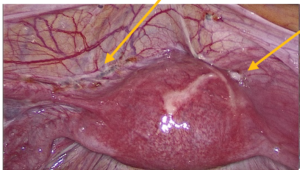
При лапароскопическом доступе на передней поверхности матки визуализирована миома диаметром 6 мм на тонком основании (тип 7, по International Federation of Gynecology and Obstetrics). На брюшине Дугласова кармана, пузырно-маточной складке — сливные очаги эндометриоза с тенденцией к инфильтративному росту (рис. 1С; 2С). Мезосальпинкс у дистального отдела левой маточной трубы со множеством очагов эндометриоза, диаметром до 7 мм, в спайках с сигмовидной кишкой (рис. 3С). Правый и левый яичники без особенностей.
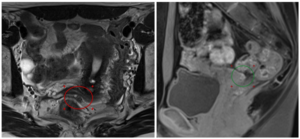
А. Б. В.
Рис. 1. Очаги эндометриоза ретроцервикально: А — МРТ, Т2-ВИ аксиальная плоскость; В — МРТ, Т2-ВИ Т1-fs-ВИ сагиттальная плоскость (фото Сергиеня О.В.); С — лапароскопический доступ (фото Маколкина А.А.).
Примечание. Здесь и в рисунках 2, 3: МРТ — магнитно-резонансная томограмма, ВИ — взвешенное изображение
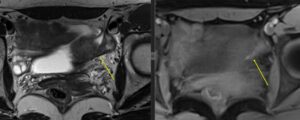
А. Б. В.
Рис. 2. Очаги эндометриоза у левой маточной трубы: А — МРТ, Т2-ВИ аксиальная плоскость; В — МРТ, Т1-fs-ВИ аксиальная плоскость (фото Сергиеня О.В.); С — лапароскопический доступ (фото Маколкина А.А.)
А. Б. В.
Рис. 3. Очаги эндометриоза маточно-пузырного углубления: А — МРТ, Т1-fs-ВИ сагиттальная плоскость; В — МРТ, Т2-ВИ сагиттальная плоскость (фото Сергиеня О.В.); С — лапароскопический доступ (фото Маколкина А.А.)
С использованием биполярной коагуляции после разделения спаек произведена миомэктомия, затем иссечены очаги эндометриоза. При хромогидроскопии обе маточные трубы проходимы. На область пузырно-маточной складки, левый мезосальпинкс, левую яичниковую ямку, дно Дугласова кармана наложен противоспаечный барьер Interceed.
Для оценки тяжести эндометриоза подсчитаны баллы, согласно пересмотренной в 1996 году классификации Американского общества фертильности (R-AFS) [10]. Глубокие эндометриоидные очаги на брюшине общей площадью более 3 см — 6 баллов (II стадия).
В результате пациентке установлен диагноз: Первичное бесплодие. Наружный генитальный эндометриоз II стадии.
При составлении дальнейшего плана лечения мы отметили, что необходимо достичь двух целей: купировать болевой синдром и преодолеть бесплодие. С учетом жалоб пациентки на хроническую тазовую боль и диспареунию принято решение о назначении гормональной терапии после операции (диеногест 2 мг/сут в ежедневном режиме). Через 2 месяца после операции на фоне терапии у больной существенно снизилась интенсивность болевого синдрома — до 1–2 баллов по ВАШ, исчезла болезненность во время полового контакта.
Шансы пары на успешное зачатие после хирургического лечения эндометриоза оценивали с помощью индекса фертильности при эндометриозе (Endometriosis Fertility Index, EFI) [11]. В нашем клиническом случае EFI — 8 баллов. Согласно данным статистики, вероятность наступления спонтанной беременности при таких показателях — 40% в течение 12 месяцев планирования [11].
Однако в этой ситуации принято решение о проведении цикла ВРТ для преодоления бесплодия в связи с длительностью заболевания, неэффективным лечением в анамнезе, наличием наружного генитального эндометриоза II стадии и желанием пациентки. Было предложено применение сегментированного протокола экстракорпорального оплодотворения с криоконсервацией всех полученных эмбрионов на фоне продолжения гормональной терапии болевого синдрома (диеногест 2 мг/сут).
Для овариальной стимуляции использовался протокол с гестагенным праймингом. На фоне приема диеногеста начата овариальная стимуляция с использованием менопаузального гонадотропина в дозе 150 МЕ/сут. Ее длительность составила 9 дней. На 11-й день стимуляции в качестве триггера овуляции введен агонист гонадотропин рилизинг-гормона трипторелин в дозе 0,2 мг/мл.
Через 36 часов после введения триггера в результате трансвагинальной пункции яичников получены 16 ооцитов. Оплодотворение производилось методом инсеминации ооцитов, получены 11 эмбрионов. Эмбрионы культивировались до 6 суток. На 5-е и 6-е сутки культивирования выполнена биопсия трофэктодермы, и криоконсервированы 6 бластоцист хорошего качества. Пациентка приняла решение о проведении предимплантационного генетического тестирования эмбрионов на анэуплоидии (ПГТ-А) с целью повышения эффективности переноса эмбрионов.
Она продолжила прием диеногеста в дозировке 2 мг в сутки после проведения пункции яичников. Через 3 месяца лечения женщина отметила выраженный клинический эффект и полное исчезновение болевого синдрома. Диеногест был отменен для подготовки к переносу эмбрионов. Через 1 месяц осуществлен перенос 1 эуплоидного эмбриона в естественном цикле, после которого наступила клиническая беременность. В настоящее время беременность прогрессирует (рис. 4).
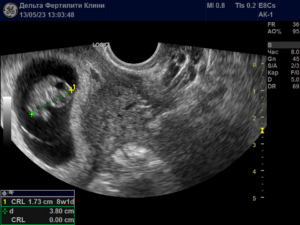
Рис. 4. Ультразвуковое исследование. Прогрессирующая маточная беременность, срок — 8 недель 1 день (иллюстрация Гореловой И.В.)
Обсуждение
На примере данного клинического случая показаны возможности современных методов неинвазивной диагностики наружного генитального эндометриоза, а также одновременного лечения двух его основных симптомов: болевого синдрома и бесплодия.
Поиск наилучших способов неинвазивной диагностики эндометриоза продолжается, но только использование методов лучевой диагностики доказало свою эффективность [7, 12]. С увеличением разрешающей способности методик повышается их эффективность в выявлении эндометриоза. Однако, по мнению ESHRE, на данный момент ни трансвагинальное УЗИ, ни МРТ пока не обладают высокой чувствительностью и специфичностью для диагностики эндометриоза любой локализации (например, при диагностике поверхностных очагов) [7]. Средняя специфичность МРТ при диагностике глубоких очагов эндометриоза малого таза составляет 77% (95% доверительный интервал (ДИ): 44–100%), а средняя чувствительность — 94% (95% ДИ: 90–97%) [12]. Для диагностики поверхностных очагов эндометриоза, по данным МРТ, в исследовании C.B. Wykes и соавт. сообщается о специфичности 72% и чувствительности 79% [13].
По результатам исследований, УЗИ обладает схожими с МРТ чувствительностью и специфичностью в выявлении глубоких очагов эндометриоза, однако такая диагностика требует аппаратуры экспертного уровня и проведения исследования опытным специалистом [7]. В описанном клиническом случае неоднократные УЗИ не позволили установить диагноз эндометриоза. По нашим данным, которые иллюстрирует история пациентки, МРТ органов малого таза обладает более высокой прогностической способностью по обнаружению очагов наружного генитального эндометриоза [14].
Очаги наружного генитального эндометриоза при МРТ определяются как имплантаты, тканевые массы или геморрагические включения в окружении фиброзной ткани, которые проявляются в виде гипоинтенсивных участков и/или гиперинтенсивных фокусов на Т1- или Т2-взвешенных МРТ-изображениях в различных локализациях малого таза. Эндометриоидные имплантаты доступны для визуализации, когда их толщина достигает 4–5 мм, из-за возможной толщины среза самого томографа [15].
Таким образом, МРТ как метод неинвазивной диагностики может и должна использоваться у пациенток с подозрением на наличие наружного генитального эндометриоза, в том числе страдающих бесплодием [16]. Достоверное обнаружение глубоких очагов эндометриоза, по данным МРТ, может внести весомый вклад в решение вопроса о необходимости проведения хирургического вмешательства. Надежность выявления эндометриоза и предварительная оценка степени поражения важны для принятия врачом решения о выборе тактики лечения бесплодия, которое должно быть взвешенным, обоснованным, а время до достижения желанной беременности — максимально коротким.
Для пациенток с эндометриозом вопрос об оптимальной овариальной стимуляции остается открытым [17]. Предложено множество стратегий стимуляций, но убедительные преимущества одного протокола перед другим не установлены [17]. До сих пор большинство опубликованных данных свидетельствовали о том, что пациенток с эндометриозом следует лечить с помощью пролонгированного протокола с использованием агонистов гонадотропин рилизинг-гормона [18]. Однако недавний обзор показал, что антагонист гонадотропин рилизинг-гормона или протокол с гестагенным праймингом могут быть более подходящими, чем протокол длительного подавления эндометриоза [19].
Профилактика преждевременного выброса лютеинизирующего гормона (ЛГ) и овуляции — неотъемлемая часть овариальной стимуляции. Назначение гестагена на протяжении всей стимуляции эффективно предотвращает всплеск ЛГ.
Несмотря на то что протокол с гестагенным праймингом был разработан относительно недавно, сведения о его эффективности и безопасности позволили включить его в рекомендации ESHRE по овариальной стимуляции в циклах ВРТ [17]. Преимуществами данного протокола являются также возможность перорального или интравагинального применения гестагенов и снижение затрат на лечение [20, 21].
Выбор гестагенов для прайминга достаточно широк. В литературе описаны протоколы с использованием микронизированного прогестерона, дидрогестерона и медроксипрогестерона ацетата [22, 23]. По данным последних исследований, в качестве гестагенного прайминга может применяться и диеногест, особенно у пациенток с эндометриозом. В проспективном когортном исследовании N. Iwami и соавт. отмечается, что доля зрелых ооцитов была значительно выше при использовании диеногеста, чем дидрогестерона (89,1% против 78,9%). Частота оплодотворения и бластуляции в обеих группах была сопоставимой [22].
Вышеперечисленные данные обусловили выбор диеногеста в качестве компонента овариальной стимуляции у нашей пациентки. Диеногест ингибирует рост эндометриоидных поражений за счет индукции децидуализации и ингибирования имплантации и ангиогенеза в эндометриоидных поражениях [24, 25], что способствует снижению риска рецидива после хирургического лечения и купированию болевого синдрома. Однако пациентки, планирующие беременность, обычно прекращают прием диеногеста до начала применения ВРТ, что может приводить к рецидиву заболевания, особенно при длительном периоде лечения бесплодия [22]. Использование диеногеста в протоколе овариальной стимуляции с гестагеновым праймингом позволяет максимально долго продолжать гормональную терапию и сократить время, в течение которого пациентка не получает противорецидивное лечение [26].
Тактика с переносом эмбриона в полость матки в сегментированном цикле была обоснована и учитывала риск развития синдрома гиперстимуляции яичников у данной пациентки (молодой возраст — 31 год, уровень АМГ — 3,2 нг/мл, получение 16 ооцитов), выбор протокола стимуляции и решение пациентки о проведении ПГТ-А эмбрионов. При использовании протокола с гестагеновым праймингом перенос эмбрионов не может быть проведен в том же цикле, что и овариальная стимуляция, в связи с отсутствием рецептивности эндометрия [17]. Перенос одного выбранного эмбриона у пациенток с эндометриозом — это уменьшение риска развития серьезных осложнений из-за тяжести ранее перенесенных операций в поздних сроках беременности и в родах [27].
Заключение
Данный клинический случай иллюстрирует современные возможности комплексной диагностики причин бесплодия с применением неинвазивных методов визуализации: МРТ органов малого таза позволила своевременно установить у пациентки этиологию бесплодия и составить план лечения. Использование гормональной терапии (диеногеста 2 мг/сут) в качестве одной из составляющих протокола овариальной стимуляции помогло купировать хронический болевой синдром, не откладывая лечение бесплодия, а также в кратчайшие сроки достичь клинической беременности.
Предыдущая статья
И.Ф. Фаткуллин ФГБОУ ВО «Казанский государственный медицинский университет» Министерства здравоох...